中国民间中医医药研究开发协会国际针灸合作委员会
办公地点现在已经搬迁至西城区西直门南小街国英园一号楼824室,
同时为方便大家联系,固定电话已经变更
新号码010―58562339。特此通知。
地址:北京西城区西直门南小街国英园一号楼824室
邮编:100035
电话:010-58562339
传真:010-58562339
邮箱:cngjzj@163.com
网站(点击网址直接链接↓):http://www.cngjzj.com/
博客(点击网址直接链接↓):http://blog.sina.com.cn/cngjzj
交通路线图 (点击观看大图)
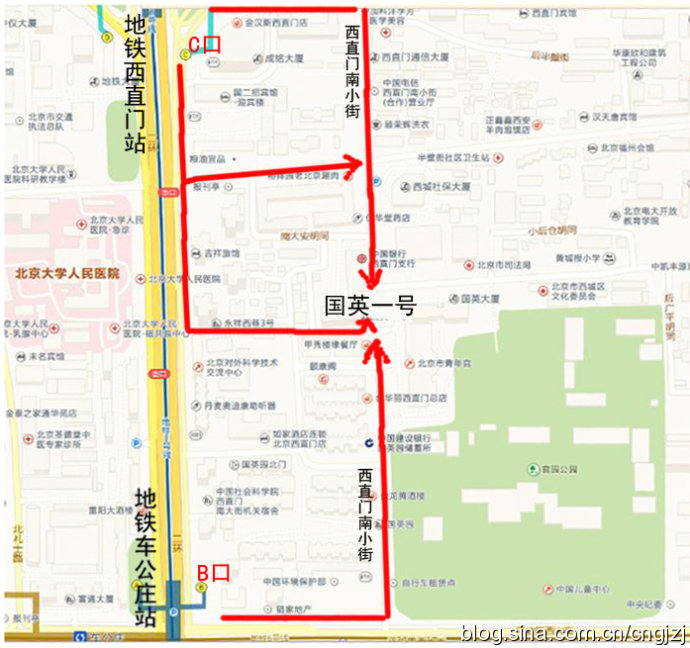
从首都机场乘坐机场专线,在东直门站下车换乘地铁2号线开往西直门方向,在西直门站 C 口出站:
1、沿西直门内大街向东直行100米,右拐到西直门南小街,向南步行到丁字路口即到国英园1号楼楼下。
2、向南直行50米,绕过 国二招宾馆 沿着中大安胡同向东到西直门南小街,向南步行到丁字路口即到国英园1号楼楼下。
从首都机场内乘坐机场直达西单的大巴,在西单站下车,乘坐出租车到西直门南小街国英园1号楼。
公交官园站:107路,运通106路
公交西直门南:387路,44路,800内环,816路,820内环,845路
地铁车公庄:地铁二号线
地铁西直门:地铁二号线
公交车公庄东:107路,118路,701路
公交车公庄北:209路,375路,392路
2016年05月17日
 复制链接
复制链接
 打印
打印
 大 中 小
大 中 小
中国仿制药可以向印度学习什么?
中国仿制药的疗效要想与原研药一致,就必须向印度药企学习,在完成一致性评价的基础上,生产质量控制全面向FD A认证对标。2014年以来,药品监管机构强力推动仿制药的质量控制,启动新的G M P认证,还要求所有厂商重新以原研药为“对标”,开展一致性评价,纠正历史误差,这将推翻大多数仿制药企业现有的生产标准和流程。这是一个利好消息,如果实施得当,可以强有力地改变目前仿制药市场的乱局。